以生活之美,啟化學之光——以“醛”的教學設計為例
作者:張運飛 李紅英
發布時間:2020-03-24 14:30:18 來源:陜西教育報刊社
一、教學背景分析
1.教材分析
“醛”是人教版化學選修五的內容,以乙醛為代表,介紹了乙醛的分子結構和物理性質,從結構引出乙醛的重要化學性質:乙醛的加成及氧化反應,這樣就自然而然地把乙醛、乙醇、乙酸串聯了起來。
2.學情分析
學生在人教版化學必修二已經學過了葡萄糖的特征反應及銀氨溶液和新制氫氧化銅懸濁液的反應,對醛基的還原性有了大概了解。在選修五中又初步接觸和掌握了烯烴和醇的性質,對有機反應中氧化還原的本質有了一定了解;對官能團決定有機物的化學性質有了一定認識,具備了根據有機物分子結構初步預測物質化學性質的簡單實驗能力。
二、教學過程設計
教學環節1.科技引領,體驗方法
新課引入:某有機物A的分子式為C2H40(A的核磁共振氫譜如圖所示),引導學生嘗試寫出結構簡式,并指認兩個吸收峰的歸屬。
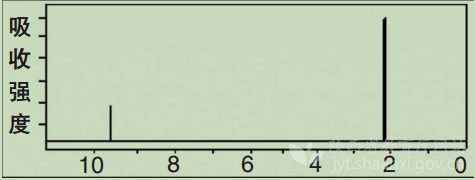
A的核磁共振氫譜
教學環節2.發現乙醛,了解乙醛
教師先用PPT展示葡萄酒及其主要成分表,引導學生發現乙醛,并思考葡萄酒中的乙醛是從哪兒來的。隨后,在PPT中引入乙醛自說,讓學生充分認識乙醛。
教學環節3.觀察模型,認知符號
教師展示乙醛的球棍模型、比例模型。學生先觀察模型,再書寫分子式、結構式和結構簡式。教師巡視學生書寫情況,并及時進行點評。
教學環節4.觀察結構,預測性質
教師讓學生觀察乙醛的分子結構,指出官能團。學生觀察后進行匯報。教師隨后提問:“醛基是很重要的官能團,請根據結構特點及所學知識預測乙醛的化學性質,可以發生什么反應?”學生進行討論,預測其性質,如具有還原性,可以發生氧化反應;具有氧化性,可以發生還原反應。
教學環節5.設計實驗,驗證性質
設計實驗:乙醛具有還原性,可以與強氧化劑高錳酸鉀反應,使高錳酸鉀酸性溶液褪色。
學生實驗1:乙醛與KMnO4酸性溶液反應。
實驗現象:KMnO4溶液褪色。
實驗結論:乙醛能被KMnO4酸性溶液氧化,說明乙醛具有還原性。
乙醛在一定溫度和催化劑存在的條件下,能被空氣中的氧氣氧化為乙酸。教師引導學生寫出該化學反應方程式,讓學生指出其斷鍵位置。隨后,教師啟發學生思考葡萄糖的特征反應,并告訴學生葡萄糖可以發生銀鏡反應,可以與新制的氫氧化銅懸濁液發生反應。
教學環節6.實驗探究,符號表達
學生實驗2:探究CH3CHO與新制Cu(0H)2懸濁液的反應。
(1)配制Cu(0H)2懸濁液。向潔凈的試管中加10%的NaOH溶液2ml,滴入4~6滴2%的CuSO4溶液,振蕩。
(2)乙醛的氧化。向Cu(0H)2懸濁液中滴入0.5 ml的乙醛溶液,振蕩后用酒精燈加熱至沸騰。
實驗現象:先出現藍色絮狀沉淀→后出現紅色沉淀。
學生認真閱讀實驗步驟,掌握實驗操作,觀察實驗現象,及時記錄。教師強調實驗操作要領及實驗安全,并提出問題:藍色沉淀是什么物質?它的反應方程式怎么表示?學生回答并書寫方程式。教師提問:紅色沉淀是什么物質?反應物是什么?反應方程式怎么表示?學生思考并書寫方程式后,教師引導、點評。
學生實驗3:探究CH3CHO與銀氨溶液的反應。
在潔凈的平底燒瓶中加入3滴管2%的AgNO3溶液,邊振蕩試管邊向其中滴入2%的稀氨水,直至生成的沉淀恰好溶解;再加入2滴管的乙醛溶液,并逐滴加入氫氧化鈉溶液,直至剛好產生沉淀,輕輕搖晃燒瓶,直至銀鏡生成。
學生要認真閱讀實驗步驟,掌握實驗操作,細心觀察實驗現象,并及時記錄實驗過程。教師應強調實驗操作要領及實驗安全,根據教材引導學生了解白色沉淀產生及消失的原理。教師向學生講解教材上關于此實驗的一句話:銀氨溶液的主要成分是Ag(NH3)2OH,它是一種弱氧化劑,能把乙醛氧轉化成乙酸,乙酸又與氨反應生成乙酸銨,而Ag+被還原成金屬銀。讓學生嘗試寫出該化學反應方程式后,教師向學生講解乙醛氧化反應的相關知識。
三、教學反思
本節課的教學設計是圍繞兩條線索進行的。一是生活線,注重學科素養教學。二是結構線,注重學生思維教學。教師應精心設計好“過渡”與“銜接”,搭建自主、合作、探究的學習平臺,將“宏觀、微觀、符號”三種認識方法融入學生學習過程,以此提升化學教學的質量。
作者單位 陜西省西安市七十中學陜西省寶雞市斗雞中學

 熱點新聞
熱點新聞
 深度報道
深度報道
 新聞視頻
新聞視頻

 投稿
投稿 APP下載
APP下載


























